Strontiumiodid
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
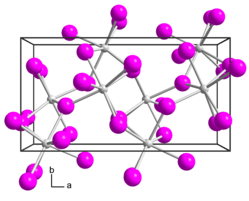 | ||||||||||||||||
| _ Sr2+ 0 _ I− | ||||||||||||||||
| Kristallsystem | orthorhombisch | |||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Strontiumiodid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | SrI2 | |||||||||||||||
| Kurzbeschreibung | farbloser, kristalliner Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 341,43 g·mol−1 | |||||||||||||||
| Aggregatzustand | fest | |||||||||||||||
| Dichte | 4,55 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | 507–645 °C[2] | |||||||||||||||
| Siedepunkt | 1773 °C (Zersetzung)[1] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Strontiumiodid (auch Strontium(II)-iodid) ist das Iodid des Erdalkalimetalls Strontium. Die Summenformel lautet SrI2.
Darstellung
Strontiumiodid kann durch Reaktion von Strontiumcarbonat mit Iodwasserstoff dargestellt werden.[6]
Eigenschaften
Es ist ein weißer, kristalliner, gut wasserlöslicher Feststoff, der sich in einem Bereich von 507 bis 645 °C verflüssigt und bei 1773 °C zersetzt wird. Die Verbindung ist hygroskopisch und verfärbt sich an der Luft gelblich. Bei hohen Temperaturen und Anwesenheit von Luft zerfällt die Verbindung komplett zu Strontiumoxid und elementarem Iod.[7]
Es existieren verschiedene Hydrate des Strontiumiodids. Das Hexahydrat SrI2 · 6 H2O gibt bei 383 K im Stickstoffstrom vier Moleküle Kristallwasser ab und geht in das Dihydrat SrI2 · 2 H2O über.[8]
| Kristallstruktur und Gitterkonstanten der Hydrate von Strontiumiodid | ||||||||
| Bezeichnung | Formel | Kristallsystem | Raumgruppe | a [pm] | b [pm] | c [pm] | β | Z |
|---|---|---|---|---|---|---|---|---|
| Anhydrat[9][10] | SrI2 | orthorhombisch | Pbca (Nr. 61)Vorlage:Raumgruppe/61 | 1522 | 822 | 790 | – | 8 |
| Dihydrat[8] | SrI2 · 2 H2O | orthorhombisch | Pcmn (Nr. 62, Stellung 4)Vorlage:Raumgruppe/62.4 | 1558,05 | 434,03 | 988,14 | – | 4 |
| Hexahydrat[11] | SrI2 · 6 H2O | trigonal | P3 (Nr. 147)Vorlage:Raumgruppe/147 | 851 | – | 429 | – | 2 |
Verwendung
Strontiumiodid wird seit einiger Zeit für Szintillator-Kristalle genutzt. Die Eigenschaften solcher Strontiumiodid-Szintillatoren sind für medizinische Zwecke und auch für sicherheitsrelevante Anwendungen erwünscht, um damit Isotope identifizieren und unterscheiden zu können.[12]
Weblinks
- Informationen bei Webelements (englisch)
Einzelnachweise
- ↑ a b c Datenblatt Strontiumiodid bei Alfa Aesar, abgerufen am 8. Mai 2010 (Seite nicht mehr abrufbar).
- ↑ Francis Turner: The Condensed Chemical Dictionary, New York, The Chemical Catalog Company, S. 449.
- ↑ a b c Datenblatt Strontium iodide bei Sigma-Aldrich, abgerufen am 23. April 2011 (PDF).
- ↑ Atherton Seidell: Solubilities Of Inorganic And Organic Substances: A Handbook Of The Most Reliable Quantitative Solubility Determinations, Kessinger Publishing, 2008, ISBN 1-4372-6497-2.
- ↑ Eintrag zu Strontium iodide in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar, Inhalt nun verfügbar via PubChem ID 25304)
- ↑ Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 923.
- ↑ E. Bartley: Text-book of Medical and Pharmaceutical Chemistry, 5. Auflage, Philadelphia, S. 267–268.
- ↑ a b W. Buchmeier, H. D. Lutz: Structure of strontium iodide dihydrate in Acta Cryst. 1986, C42, S. 651–653, doi:10.1107/S0108270186095045
- ↑ E. Th. Rietschel, H. Bärnighausen: Die Kristallstruktur von Strontiumiodid SrI2. In: Zeitschrift für anorganische und allgemeine Chemie, 368, 1969, S. 62–72, doi:10.1002/zaac.19693680110.
- ↑ Es ist auch eine metastabile Phase mit der Raumgruppe Pnma (Nr. 62)Vorlage:Raumgruppe/62 bekannt (G. Liu, H.A. Eick: The Structure of a Metastable Form of SrI2 By the X-Ray Rietveld Procedure. In: Journal of the Less-Common Metals, 156, 1989, S. 237–245, doi:10.1016/0022-5088(89)90422-0).
- ↑ Z. Herrmann: Über die Strukturen der Strontiumjodid-, Calciumchlorid- und Calciumbromid-Hexahydrate in Zeitschrift für anorganische und allgemeine Chemie 1931, 197(1), S. 212–218. doi:10.1002/zaac.19311970118
- ↑ LLNL Industrial Partnerships Office (IPO): Strontium Iodide Scintillator Detector (Memento vom 16. Februar 2013 im Internet Archive).










