Hipobromit
 | Ezt a szócikket át kellene olvasni, ellenőrizni a szöveg helyesírását és nyelvhelyességét, a tulajdonnevek átírását. Esetleges további megjegyzések a vitalapon. |
| Hipobromit | |||
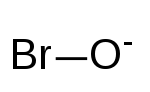 | |||
| IUPAC-név | hipobromit | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| PubChem | 5460626 | ||
| ChemSpider | 4574121 | ||
| ChEBI | 29250 | ||
| |||
| InChIKey | JGJLWPGRMCADHB-UHFFFAOYSA-N | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | BrO− | ||
| Moláris tömeg | 95,904 g/mol | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A hipobromit szervetlen anion, melynek képlete BrO−. Benne a bróm oxidációs száma +1. Analóg a hipoklorittal. A hipoklorithoz hasonlóan használják csíraölőként és parazitaellenes szerként, és az immunsejtekben is megtalálható. A hipobromitok a hipobrómossav sói.
Előállítása
Bróm és vízben oldott hidroxid (például nátrium- vagy kálium-hidroxid) reakciójával:[1]
- Br2 + 2OH− → Br− + BrO− + H2O
A fenti reakcióban a bróm diszproporcionálódik.
A másodlagos reakcióban a hipobromit spontán diszproporcionálódik bromiddá (oxidációs száma −1) és bromáttá (oxidációs száma +5), a reakció gyorsan játszódik le 20 °C-on, és lassan 0 °C-on:
- 3BrO− → 2Br− + BrO−3
A reakció analóg a hipoklorit klorid és kloráttá bomlásához.
A hipobromit sókat ki lehet kristályosítani:
Előfordulása
Jelen van a vérben az eozinofil sejtekben, parazitaellenes szerként, többsejtű paraziták ellen.[2] Egyszerű bromid sókban (például nátrium-bromid) használják gyógyfürdőkben fertőtlenítő szerként, amikből oxidálószer például hidrogén-peroxid hatására hipobromit keletkezik. Használják a laboratóriumokban reagensként a Hofmann-lebontásnál, amikben karboxamidokból primer aminok keletkeznek.[3]
Kapcsolódó szócikkek
- Bromid: Br−
- Bromit: BrO−2
- Bromát: BrO−3
- Perbromát: BrO−4
Jegyzetek
- ↑ The Halogens, Chemistry. Facts, Patterns and Principles. Addison-Wesley (1972). ISBN 0-201-03779-3
- ↑ Mayeno AF, Curran AJ, Roberts RL, Foote CS (1989. április 5.). „Eosinophils preferentially use bromide to generate halogenating agents”. Journal of Biological Chemistry 264 (10), 5660–5668. o. [2021. március 7-i dátummal az eredetiből archiválva]. (Hozzáférés: 2024. január 29.)
- ↑ Siegfried Hauptmann: Organische Chemie, Verlag Harry Deutsch, Thun (1985) S. 423, ISBN 3-87144-902-4.
Fordítás
- Ez a szócikk részben vagy egészben a Hypobromite című német Wikipédia-szócikk fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
- Ez a szócikk részben vagy egészben a Hypobromite című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.











