Kadmium asetat
 | |
| Nama | |
|---|---|
| Nama IUPAC Kadmium asetat | |
| Nama lain Kadmium diasetat | |
| Penanda | |
Nomor CAS |
|
Model 3D (JSmol) |
|
| 3DMet | {{{3DMet}}} |
| ChemSpider |
|
| Nomor EC | |
PubChem CID |
|
| Nomor RTECS | {{{value}}} |
| UNII |
|
CompTox Dashboard (EPA) |
|
InChI
| |
SMILES
| |
| Sifat | |
Rumus kimia | Cd(CH3COO)2 (anhidrat) Cd(CH3COO)2·2H2O (dihidrat) |
| Massa molar | 230.500 g/mol (anhidrat) 266.529 g/mol (dihidrat) |
| Penampilan | Kristal tidak berwarna (anhidrat) Kristal putih (dihidrat) |
| Bau | Asam asetat |
| Densitas | 2.341 g/cm3 (anhidrat) 2.01 g/cm3 (dihidrat) |
| Titik lebur | 255 °C (491 °F; 528 K) (anhidrat) dihidrat berdekomposisi pada suhu 130 °C [1] |
Kelarutan dalam air | Dapat larut (anhidrat), sangat mudah larut (dihidrat) |
| Kelarutan | Dapat larut dalam metanol, etanol (anhidrat) dapat larut dalam etanol (dihidrat) |
| -83.7·10−6 cm3/mol | |
| Struktur | |
| monoklinik | |
| Bahaya | |
| Frasa-R | R20/21/22 |
| Frasa-S | S2 S22[2] |
| Batas imbas kesehatan AS (NIOSH): | |
PEL (yang diperbolehkan) | [1910.1027] TWA 0.005 mg/m3 (sebagai Cd)[3] |
REL (yang direkomendasikan) | Ca[3] |
IDLH (langsung berbahaya) | Ca [9 mg/m3 (as Cd)][3] |
| Senyawa terkait | |
Anion lain | Kadmium fluorida Kadmium klorida Kadmium bromida Kadmium iodida |
Kation lainnya | Seng asetat Raksa(II) asetat Perak asetat |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
 N verifikasi (apa ini N verifikasi (apa ini  Y Y N ?) N ?) | |
| Referensi | |
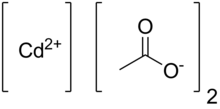
Kadmium asetat adalah senyawa kimia dengan rumus Cd(CH3CO2)2. Senyawa padat tidak berwarna ini digolongkan sebagai polimer koordinasi yang terdiri dari ligan asetat yang terhubung dengan kadmium di pusatnya. Senyawa ini ada dalam bentuk anhidrat dan dihidrat. Senyawa ini terbentuk dari reaksi kadmium oksida dengan asam asetat:[2][4]
- CdO + 2 CH3COOH → Cd(CH3COO)2 + H2O
Referensi
- ^ Lide, David R. (1998). Handbook of Chemistry and Physics (edisi ke-87). Boca Raton, Florida: CRC Press. hlm. 447. ISBN 0-8493-0594-2.
- ^ a b Gangolli, S. (1999). The Dictionary of Substances and Their Effects. London: Royal Society of Chemistry. hlm. 12–13. Diakses tanggal 2009-03-29.
- ^ a b c "NIOSH Pocket Guide to Chemical Hazards #0087". National Institute for Occupational Safety and Health (NIOSH).
- ^ Patnaik, Pradyot (2003). Handbook of Inorganic Chemical Compounds. McGraw-Hill Professional. hlm. 143–144. ISBN 0-07-049439-8. Diakses tanggal 2009-03-29.
- l
- b
- s









