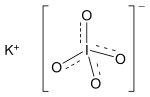
Kalium periodat
 | |
 | |
| Nama | |
|---|---|
| Nama IUPAC Kalium periodat | |
| Nama lain kaliuk metaperiodat | |
| Penanda | |
Nomor CAS |
|
Model 3D (JSmol) |
|
| 3DMet | {{{3DMet}}} |
| ChemSpider |
|
| Nomor EC | |
PubChem CID |
|
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA) |
|
InChI
| |
SMILES
| |
| Sifat | |
Rumus kimia | KIO4 |
| Massa molar | 230.00 g mol−1 |
| Penampilan | serbuk putih |
| Bau | tidak berbau |
| Densitas | 3.618 g/cm3 |
| Titik lebur | 582 °C (1.080 °F; 855 K) (terurai) |
Kelarutan dalam air | 0.17 g/100 mL (0 °C) 0.42 g/100 mL (20 °C) 4.44 g/100 mL (80 °C) 7.87 g/100 mL (100 °C) |
| Struktur | |
Struktur kristal | tetragonal |
| Bahaya | |
| Bahaya utama | Oksidan |
| Lembar data keselamatan | External MSDS |
| Senyawa terkait | |
Anion lain | Kalium iodida Kalium iodat |
Kation lainnya | Natrium periodat |
Senyawa terkait | Asam periodat |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
 Y verifikasi (apa ini Y verifikasi (apa ini  Y Y N ?) N ?) | |
| Referensi | |
Kalium periodat adalah garam anorganik dengan rumus kimia KIO4. Ini terdiri dari kation kalium dan anion periodat dan dapat juga dianggap sebagai garam kalium dari asam periodat. Perhatikan bahwa pelafalannya adalah per-iodat, bukan period-at.
Tidak seperti periodat umum lainnya, seperti natrium periodat dan asam periodat, itu hanya tersedia dalam bentuk metaperiodat; kalium ortoperiodat (K5IO6) yang sesuai belum pernah dilaporkan.
Persiapan
Kalium periodat dapat dibuat dengan oksidasi larutan kalium iodat dalam air oleh klorin dan kalium hidroksida.[1]
Ini juga dapat dihasilkan oleh oksidasi elektrokimia dari kalium iodat, namun kelarutan yang rendah dari KIO3 membuat pendekatan ini penggunaan terbatas.
Sifat kimia
Kalium periodat terurai pada 582 °C untuk membentuk kalium iodat dan oksigen.
Kelarutan KIO4 yang rendah membuatnya berguna untuk penentuan kalium dan serium.
Ini sedikit larut dalam air (salah satu garam kalium yang kurang larut, karena anion besar), sehingga memunculkan larutan yang sedikit basa. Pada pemanasan (terutama dengan mangan(IV) oksida sebagai katalis), ia terurai untuk membentuk kalium iodat, melepaskan gas oksigen.
KIO4 membentuk kristal tetragonal dari tipe Scheelite (grup ruang I41/a).[2]
Referensi
- ^ Riley, edited by Georg Brauer ; translated by Scripta Technica, Inc. Translation editor Reed F. (1963). Handbook of preparative inorganic chemistry. Volume 1 (edisi ke-2nd). New York, N.Y.: Academic Press. hlm. 325. ISBN 978-0121266011. Pemeliharaan CS1: Teks tambahan: authors list (link)
- ^ Al-Dhahir, T.A.; Dhanaraj, G.; Bhat, H.L. (June 1992). "Growth of alkali metal periodates from silica gel and their characterization". Journal of Crystal Growth. 121 (1-2): 132–140. doi:10.1016/0022-0248(92)90182-I.
- l
- b
- s
- KAsO2
- KBr
- KBrO3
- KCN
- KCNO
- KCl
- KClO3
- KClO4
- KF
- KH
- KHCO2
- KHCO3
- KHF2
- KHS
- KHSO3
- KHSO4
- KH2AsO4
- KH2PO3
- KH2PO4
- KI
- KIO3
- KIO4
- KMnO4
- KN3
- KNH2
- KNO2
- KNO3
- KOCN
- KOH
- KO2
- KPF6
- KSCN
- KCH3COO
- K2Al2O4
- K2CO3
- K2CrO4
- K2Cr2O7
- K2FeO4
- K2HPO4
- K2MnO4
- K2O
- K2O2
- K2PtCl4
- K2PtCl6
- K2S
- K2SeO4
- K2SO3
- K2SO4
- KHSO5
- K2S2O5
- K2S2O7
- K2S2O8
- K2Po
- K2SiO3
- K3[Fe(CN)6]
- K3[Fe(C2O4)3]
- K4[Fe(CN)6]
- K3PO4
- K4Mo2Cl8
 | Artikel bertopik kimia ini adalah sebuah rintisan. Anda dapat membantu Wikipedia dengan mengembangkannya. |
- l
- b
- s










