Kobalt(II) klorida
| |||
 Struktur senyawa anhidrat | |||
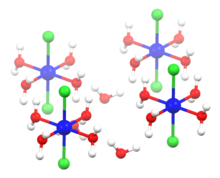 Struktur heksahidrat | |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC Cobalt(II) chloride | |||
| Nama lain Cobaltous chloride Kobalt diklorid Muriat kobalt[1] | |||
| Penanda | |||
Nomor CAS |
| ||
Model 3D (JSmol) |
| ||
| 3DMet | {{{3DMet}}} | ||
| ChEBI |
| ||
| ChemSpider |
| ||
| Nomor EC | |||
PubChem CID |
| ||
| Nomor RTECS | {{{value}}} | ||
| UNII |
| ||
| Nomor UN | 3288 | ||
CompTox Dashboard (EPA) |
| ||
InChI
| |||
SMILES
| |||
| Sifat | |||
Rumus kimia | CoCl2 | ||
| Massa molar | 129.839 g/mol (anhidrat) 165.87 g/mol (dihidrat) 237.93 g/mol (heksahidrat) | ||
| Penampilan | kristal biru (anhidrat) ungu-kebiruan (dihidrat) kristal merah mawar (heksahidrat) | ||
| Densitas | 3.356 g/cm3 (anhidrat) 2.477 g/cm3 (dihidrat) 1.924 g/cm3 (heksahidrat) | ||
| Titik lebur | 726 °C (1.339 °F; 999 K) ±2 (anhidrat) 140 °C (monohidrat) 100 °C (dihidrat) 86 °C (heksahidrat) | ||
| Titik didih | 1.049 °C (1.920 °F; 1.322 K) | ||
Kelarutan dalam air | 43.6 g/100 mL (0 °C) 45 g/100 mL (7 °C) 52.9 g/100 mL (20 °C) 105 g/100 mL (96 °C) | ||
| Kelarutan | 38.5 g/100 mL (metanol) 8.6 g/100 mL (aseton) larut dalam etanol, pyridine, gliserol | ||
| +12,660·10−6 cm3/mol | |||
| Struktur | |||
| CdCl2 structure | |||
| heksagonal (anhidrat) monoklinik (dihidrat) Oktahedral (heksahidrat) | |||
| Bahaya | |||
| Lembar data keselamatan | ICSC 0783 | ||
| Piktogram GHS |    | ||
| Titik nyala | Tidak mudah terbakar | ||
| Dosis atau konsentrasi letal (LD, LC): | |||
LD50 (dosis median) | 80 mg/kg (tikus, mulut) | ||
| Senyawa terkait | |||
Anion lain | Kobalt(II) fluorida Kobalt(II) bromida Kobalt(II) iodida | ||
Kation lainnya | Rhodium(III) klorida Iridium(III) klorida | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
 N verifikasi (apa ini N verifikasi (apa ini  Y Y N ?) N ?) | |||
| Referensi | |||
Kobalt(II) Klorida merupakan sebuah senyawa anorganik yang tersusun dari kobalt dan klorin, dengan rumus kimia CoCl2. Ini berpenampilan padatan kristal biru langit.
Senyawa ini membentuk beberapa hidrat, CoCl2•nH2O, untuk n = 1, 2, 6, dan 9. Klaim pembentukan tri- dan tetrahidrat tidak terkonfirmasi.[3] Senyawa dihidrat berwarna ungu dan heksahidrat berwarna merah muda. Senyawa ini biasa diedarkan sebagai heksahidrat CoCl2·6H2O, termasuk senyawa kobalt yang banyak digunakan dalam laboratorium.[4]
Referensi
- ^ "Cobalt muriate, CAS Number: 7646-79-9". www.chemindustry.com. Diarsipkan dari versi asli tanggal 2019-05-28. Diakses tanggal 19 April 2018.
- ^ Santa Cruz Biotechnology: Cobalt(II) chloride
- ^ M. T. Saugier, M. Noailly, R. Cohen-Adad, F. Paulik, and J. Paulik (1977): "Equilibres solide ⇄ liquide ⇆ vapeur du systeme binaire CoCl2-H2O" Journal of Thermal Analysis, volume 11, issue 1, pages 87–100. DOI:10.1007/BF02104087 Note: the lowest point of fig.6 is inconsistent with fig.7; probably should be at -27.8 C instead of 0 C.
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4 Pemeliharaan CS1: Banyak nama: authors list (link)

Wikimedia Commons memiliki media mengenai cobalt(II) chloride.
- International Chemical Safety Card 0783
- National Pollutant Inventory – Cobalt fact sheet Diarsipkan 2006-02-19 di Wayback Machine.
- IARC Monograph "Cobalt and Cobalt Compounds"
- l
- b
- s
Senyawa kobalt
- CoBr2
- Co(CN)2
- CoCO3
- CoC2O4
- CoCl2
- CoCl3
- Co(ClO3)2
- CoF2
- CoF3
- CoI2
- Co(NO3)2
- Co(NO3)3
- CoO
- Co(OH)2
- CoS
- CoSO4
- CoSe
- Co2O3
- Co2P
- Co3O4
- Co3(PO4)2
- l
- b
- s
Garam dan derivat kovalen ion klorida
| HCl | He | ||||||||||||||||
| LiCl | BeCl2 | BCl3 B2Cl4 | CCl4 | NCl3 ClN3 | Cl2O ClO2 Cl2O7 | ClF ClF3 ClF5 | Ne | ||||||||||
| NaCl | MgCl2 | AlCl AlCl3 | SiCl4 | P2Cl4 PCl3 PCl5 | S2Cl2 SCl2 SCl4 | Cl2 | Ar | ||||||||||
| KCl | CaCl CaCl2 | ScCl3 | TiCl2 TiCl3 TiCl4 | VCl2 VCl3 VCl4 VCl5 | CrCl2 CrCl3 CrCl4 | MnCl2 | FeCl2 FeCl3 | CoCl2 CoCl3 | NiCl2 | CuCl CuCl2 | ZnCl2 | GaCl2 GaCl3 | GeCl2 GeCl4 | AsCl3 AsCl5 | Se2Cl2 SeCl4 | BrCl | KrCl |
| RbCl | SrCl2 | YCl3 | ZrCl3 ZrCl4 | NbCl4 NbCl5 | MoCl2 MoCl3 MoCl4 MoCl5 MoCl6 | TcCl4 | RuCl3 | RhCl3 | PdCl2 | AgCl | CdCl2 | InCl InCl2 InCl3 | SnCl2 SnCl4 | SbCl3 SbCl5 | Te3Cl2 TeCl4 | ICl ICl3 | XeCl XeCl2 |
| CsCl | BaCl2 | HfCl4 | TaCl5 | WCl2 WCl3 WCl4 WCl5 WCl6 | Re3Cl9 ReCl4 ReCl5 ReCl6 | OsCl4 | IrCl2 IrCl3 IrCl4 | PtCl2 PtCl4 | AuCl AuCl3 | Hg2Cl2, HgCl2 | TlCl | PbCl2, PbCl4 | BiCl3 | PoCl2, PoCl4 | AtCl | RnCl2 | |
| FrCl | RaCl2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| ↓ | |||||||||||||||||
| LaCl3 | CeCl3 | PrCl3 | NdCl2, NdCl3 | PmCl3 | SmCl2, SmCl3 | EuCl2, EuCl3 | GdCl3 | TbCl3 | DyCl2, DyCl3 | HoCl3 | ErCl3 | TmCl2 TmCl3 | YbCl2 YbCl3 | LuCl3 | |||
| AcCl3 | ThCl4 | PaCl5 | UCl3 UCl4 UCl5 UCl6 | NpCl4 | PuCl3 | AmCl2 AmCl3 | CmCl3 | BkCl3 | CfCl3 | EsCl3 | Fm | Md | No | LrCl3 | |||










