Dikoolstofmonoxide
| Dikoolstofmonoxide | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
 | ||||
Structuurformule van dikoolstofmonoxide | ||||
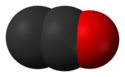 | ||||
| Algemeen | ||||
| Molecuulformule | ||||
| IUPAC-naam | 2-Oxoethenylideen | |||
| Andere namen | Ketenylideen | |||
| Molmassa | 40,021 g/mol | |||
| SMILES | [C]=C=O | |||
| InChI | 1S/C2O/c1-2-3 | |||
| CAS-nummer | 119754-08-4 | |||
| PubChem | 189691 | |||
| Wikidata | Q2741198 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
Dikoolstofmonoxide, , is een chemische verbinding waarvan de moleculen uit twee koolstof-atomen en één zuurstof-atoom bestaan. Het molecuul is lineair, en vanwege zijn eenvoud is het een interessante verbinding in verschillende deelgebieden van de scheikunde. De stof is echter ook extreem reactief, zodat hij in het gewone leven van de chemicus niet voorkomt. De stof kan beschreven worden als een cumuleen en als een koolstofoxide.[1]
Synthese en voorkomen
In de literatuur zijn verschillende synthese-methoden voor dikoolstofmonoxide beschreven:
- als product van de fotolyse van koolstofsuboxide:[2][3]
- De omgekeerde reactie is ook mogelijk, daarbij ontstaat koolstofsuboxide uit en .
- als bijproduct in de radiolyse van koolstofdioxide. de reactie verloopt in een aantal stappen:[4]
Ondanks zijn instabiliteit bestaat het molecuul lang genoeg om de reacties ervan met stikstofmonoxide en stikstofdioxide te kunnen bestuderen.[5]
Onder de naam ketenylideen is de verbinding in de organometaalchemie bekend als ligand in metaal-carbonylcomplexen, bijvoorbeeld: . ketenylidenen worden voorgesteld als intermediairen in het Fischer-Tropsch-proces waarin koolstofmonoxide en waterstof worden omgezet in brandstoffen op basis van koolwaterstoffen.[6]
De organofosforverbinding (CAS# 15596-07-3) bevat het structuurelement van dikoolstofmonoxide. Deze gele vaste stof wordt soms aangeduid als "Bestmann's ylide".[7]
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Dicarbon monoxide op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- De sectie Synthese via radiolyse van koolstofdioxide of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Radiolyse op de Duitstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- Verwijzingen in de tekst
- ↑ Frenking, Gernot; Tonner, Ralf "Divalent carbon(0) compounds" Pure and Applied Chemistry 2009, vol. 81, pp. 597-614. DOI:10.1351/PAC-CON-08-11-03
- ↑ Bayes, K. (1961). Photolysis of Carbon Suboxide. Journal of the American Chemical Society 83 (17): 3712–3713. DOI: 10.1021/ja01478a033.
- ↑ Anderson, D. J., Rosenfeld, R. N. (1991). Photodissociation of Carbon Suboxide. Journal of Chemical Physics 94 (12): 7857–7867. DOI: 10.1063/1.460121.
- ↑ Ibrahim Dincer, Calin Zamfirescu: Sustainable Hydrogen Production. Elsevier, 2016, ISBN 0-12-801748-1, S. 417.
- ↑ Thweatt, W. D., Erickson, M. A., Hershberger, J. F. (2004). Kinetics of the CCO + NO and CCO + NO2 reactions. Journal of Physical Chemistry A 108 (1): 74–79. DOI: 10.1021/jp0304125.
- ↑ Jensen, Michael P.; Shriver, Duward F. "Carbon-carbon and carbonyl transformations in ketenylidene cluster compounds" Journal of Molecular Catalysis 1992, vol. 74, pp. 73-84. DOI:10.1016/0304-5102(92)80225-6
- ↑ H. J. Bestmann, R. Zimmermann, M. Riou "Ketenylidenetriphenylphosphorane" e-EROS Encyclopedia of Reagents for Organic Synthesis 2001. DOI: 10.1002/047084289X.rk005.pub2


![{\displaystyle {\ce {C3O2\ ->[{\ce {h\nu }}][{\ce {\ }}]\ CO\ +\ C2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4d2bf8420f6d4ac5c5fecb2a129d181675f4387f)

![{\displaystyle {\ce {CO2\ ->[{\ce {\gamma }}][{\ce {\ }}]\ CO\ +\ O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b80860cd071c558749763ea819455565108c521e)
![{\displaystyle {\ce {CO2\ ->[{\ce {\gamma }}][{\ce {\ }}]\ C\ +\ 2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/13c58cf781b6685e5abb12dced44bc683db41375)

![{\displaystyle {\ce {[OC2Co3(CO)9]^{+}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b7b65dfe7967ae98217a3bc6770861bd6f7d0941)








