Análise retrossintética
Análise retrossintética é uma técnica para resolver problemas no planejamento de sínteses orgânicas. Isto é conseguido através da transformação de uma molécula alvo em estruturas precursoras mais simples, sem hipóteses quanto aos materiais iniciais. Cada material precursor é examinado usando o mesmo método. Esse procedimento é repetido até estruturas simples ou comercialmente disponíveis serem alcançadas. E.J. Corey formalizou este conceito em seu livro The Logic of Chemical Synthesis.[1][2][3]
O poder da análise retrossintética torna-se evidente no projeto de uma síntese. O objetivo da análise retrossintética é a simplificação estrutural. Muitas vezes, uma síntese terá mais de uma possível rota sintética. Retrossíntese é adequada para descobrir diferentes rotas e compará-las de forma lógica e direta.[4] Um banco de dados pode ser consultado em cada etapa da análise, para determinar se um componente já existe na literatura. Nesse caso, não será necessário mais exploração desse composto.
Definições
- Desconexão
- Uma etapa retrossintética envolvendo a quebra de uma ligação para formar dois(ou mais) sintons.
- Retron
- Uma subestrutura molecular mínima que possibilita certas transformações.
- Árvore retrossintética
- Um grafo acíclico dirigido de várias (ou todas) retrossínteses possíveis de um único produto meta (alvo).
- Sinton
- Um fragmento molecular idealizado. Um sinton e o comercialmente disponível “equivalente sintético” correspondente são mostrados abaixo:
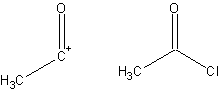
- Alvo (ou Meta)
- O composto final desejado.
- Transformado (ou ainda “trans-forma”, uma forma intermediária)
- O reverso de uma reação sintética; a formação de materiais de partida de um produto único.
Exemplo
Um exemplo permitirá que o conceito de análise retrossintética seja facilmente compreendido.
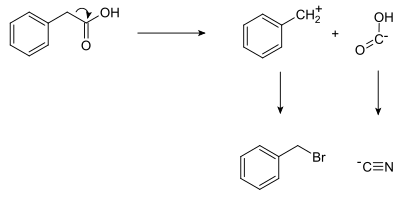
No planejamento da síntese de ácido fenilacético, dois sintons são identificados. Um grupo nucleofílico "-COOH" , e um grupo eletrofílico "PhCH2+". Evidentemente, ambos os sintons não existem per se; equivalentes sintéticos correspondentes aos sintons são colocados em reação para produzir o produto desejado. neste caso o ânion cianeto é o equivalente sintético para o sinton −COOH , enquanto brometo de benzila é o equivalente sintético para o sinton benzilo.
A síntese de ácido fenilacético determinada por análise retrossintética é então:
- PhCH2Br + NaCN → PhCH2CN + NaBr
- PhCH2CN + 2 H2O → PhCH2COOH + NH3

De fato, ácido fenilacético tem sido sintetizado do cianeto de benzila,[5] que por sua vez é é preparado por reação análoga do cloreto de benzila com cianeto de sódio.[6]
Estratégias
Estratégias de grupos funcionais
Manipulação de grupos funcionais podem conduzir a reduções significativas na complexidade molecular.
Estratégias estereoquímicas
Numerosas substâncias químicas alvos químicos tem distintas demandas estereoquímicas. Transformações estereoquímicas (tais como o rearranjo de Claisen e a reação de Mitsunobu) podem remover ou transferir a quiralidade desejada simplificando então o processo de atingir-se o alvo.
Estratégias de estrutura objetivo
Dirigir uma síntese em direção a um intermediário desejável pode reduzir muito o foco de uma análise. Isso permite técnicas de pesquisa bidirecionais.
Estratégias baseadas em transformados
A aplicação de transformações à análise retrossintética pode levar a poderosas reduções na complexidade molecular. Infelizmente, retrons baseados em transformados poderosos são raramente presentes em moléculas complexas, e etapas sintéticas adicionais são frequentemente necessárias para estabilizar sua presença.
Estratégias topológicas
A identificação de uma ou mais desconexões de ligações chave pode levar à identificação de subestruturas chave ou dificuldade de identificar transformações por rearranjos de maneira a identificar as estruturas chave.
- Desconexões que preservam estruturas em anel são encorajadas.
- Desconexões que criam anéis maiores que 7 membros são desencorajadas.
Referências
- ↑ E. J. Corey, X-M. Cheng (1995). The Logic of Chemical Synthesis. New York: Wiley. ISBN 0-471-11594-0
- ↑ E. J. Corey (1988). «Retrosynthetic Thinking - Essentials and Examples». Chem. Soc. Rev. 17: 111–133. doi:10.1039/CS9881700111
- ↑ E. J. Corey (1991). «The Logic of Chemical Synthesis: Multistep Synthesis of Complex Carbogenic Molecules (Nobel Lecture)» (Reprint). Angewandte Chemie International Edition in English. 30 (5): 455–465. doi:10.1002/anie.199104553
- ↑ James Law et.al:"Route Designer: A Retrosynthetic Analysis Tool Utilizing Automated Retrosynthetic Rule Generation", Journal of Chemical Information and Modelling (ACS JCIM) Publication Date (Web): February 6, 2009; doi:10.1021/ci800228y , http://pubs.acs.org/doi/abs/10.1021/ci800228y
- ↑ Wilhelm Wenner (1963). «Phenylacetamide». Org. Synth. ; Coll. Vol., 4
- ↑ Roger Adams; A. F. Thal (1941). «Benzyl Cyanide». Org. Synth. ; Coll. Vol., 1
Ligações externas
- Centre for Molecular and Biomolecular Informatics (Centro para Informática Molecular e Biomolecular)
- Retrosynthesis planning tool: ICSynth por InfoChem (Ferramenta de planejamento em retrossíntese)












