Etanolamină
| Etanolamină | |
 | |
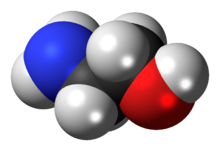 | |
| Nume IUPAC | 2-aminoetanol |
|---|---|
| Identificare | |
SMILES C(CO)N | |
| Număr CAS | 141-43-5 |
| ChEMBL | CHEMBL104943 |
| PubChem CID | 700 |
| Informații generale | |
| Formulă chimică | C2H7NO |
| Aspect | lichid incolor vâscos |
| Masă molară | 61,08 g/mol |
| Proprietăți | |
| Densitate | 1,012 g/cm3 |
| Punct de topire | 10,3 °C |
| Punct de fierbere | 170 °C |
| Solubilitate în apă | |
| miscibil | |
| Miros | miros de amoniac |
| Presiune de vapori | 0 mm Hg[1]  |
| Indice de refracție(nD) | 1,4539  |
| Viscozitate | dinamică 0 poiseuille  |
| Pericol | |
  | |
| Fraze R | R20, R34, R36/37/38 |
| Fraze S | S26, S27, S36/37, S39, S45 |
 Pericol H302 : Nocif en cas d'ingestion H312 : Nocif par contact cutané H314 : Provoque de graves brûlures de la peau et des lésions oculaires H332 : Nocif par inhalation H335 : Peut irriter les voies respiratoires P261 : Éviter de respirer les poussières/fumées/gaz/brouillards/vapeurs/aérosols. P280 : Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage. P305 : EN CAS DE CONTACT AVEC LES YEUX : P308 : EN CAS d’exposition prouvée ou suspectée : P313 : Consulter un médecin. P338 : Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer. P351 : Rincer avec précaution à l’eau pendant plusieurs minutes. | |
| NFPA 704 | |
2 3 0 | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
Modifică date / text  | |
Etanolamina, cunoscută și sub denumirile de 2-aminoetanol sau monoetanolamină, este un compus organic din clasa aminoalcoolilor, cu formula HO-CH2-CH2-NH2. Din punct de vedere chimic, este atât un alcool primar, cât și o amină primară, datorită grupărilor hidroxil și amino. Este un compus incolor, lichid și vâscos, cu un miros asemănător amoniacului. Derivații săi sunt larg răspândiți în natură, cum este de exemplu cazul lipidelor.
Obținere
La nivel industrial, monoetanolamina este obținută în urma reacției dintre oxidul de etilenă și amoniac în soluție apoasă. În urma reacției se obțin și produși secundari, anume dietanolamina și trietanolamina.[2]
Biosinteză
În organism, etanolamina este biosintetizată în urma procesului de decarboxilare a serinei:[3]
Utilizări
Etanolamina este utilizată pentru a obține etilendiamină, în urma reacției cu amoniacul:[2]

Referințe
- ^ http://www.cdc.gov/niosh/npg/npgd0256.html Lipsește sau este vid:
|title=(ajutor) - ^ a b Klaus Weissermel; Hans-Jürgen Arpe; Charlet R. Lindley; Stephen Hawkins (). „Chap. 7. Oxidation Products of Ethylene”. Industrial Organic Chemistry. Wiley-VCH. pp. 159–161. ISBN 3-527-30578-5.
- ^ „Phosphatidylethanolamine and related lipids”. AOCS. Arhivat din original la . Accesat în .















