Aluminijum oksid
| Aluminijum oksid | |||
|---|---|---|---|
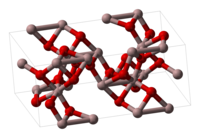 | |||
| Identifikacija | |||
| CAS registarski broj | 1344-28-1  Y Y | ||
| MeSH | aluminium+oxide | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molarna masa | 101.96 g/mol | ||
| Gustina | 3.97 g cm−3, osnovno | ||
| Tačka topljenja | 2054 °C | ||
| Tačka ključanja | 2980 °C | ||
| Rastvorljivost u vodi | nerastvoran | ||
| Struktura | |||
| Geometrija molekula | oktaedar | ||
| Termohemija | |||
| Standardna entalpija stvaranja jedinjenja ΔfH | −1675.7 kJ mol−1 | ||
| Standardna molarna entropija S | 50.92 J mol−1 K−1 | ||
| Opasnost | |||
| EU-klasifikacija | Nije na listi | ||
| Tačka paljenja | ne gori | ||
| Srodna jedinjenja | |||
| Drugi anjoni | aluminijum-hidroksid | ||
| Drugi katjoni | bor-trioksid galijum-oksid indijum-oksid talijum-oksid | ||
|
| |||
| Infobox references | |||
Aluminijum oksid (Al2O3) je neorgansko hemijsko jedinjenje aluminijuma koje se javlja u dve modifikacije:[1][2]
- α-Al2O3 (korund) je postojanija modifikacija, koja se odlikuje velikom tvrdoćom (9 stepeni u Mosovoj skali. Njegova temperatura topljenja iznosi 2040 °C, a temperatura ključanja 3300 °C. Dobro provodi toplotu, otporan je na dejstvo hemijskih supstancija, ne rastvara se u kiselinama. Nastaje usled prženja na 1000 °C modifikacije &gamma.
- γ-Al2O3 je beli prah nerastvorljiv u vodi a rastvorljiv u jakim kiselinama. Dobija se prženjem aluminijum hidroksida. Ima amfoterne osobine. Iz njega se elektrohemijskom metodom dobija metalni aluminijum.
Aluminijum oksid je glavni sastojak boksita najvažnije rude aluminijuma
Reference
Povezano
Spoljašnje veze

Aluminijum oksid na Wikimedijinoj ostavi








 Aluminijum_oksid
Aluminijum_oksid