Fosfoglicerat kinaza
| Fosfoglicerat kinaza | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Identifikatori | |||||||||
| EC broj | 2.7.2.3 | ||||||||
| CAS broj | 9001-83-6 | ||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | metabolic pathway | ||||||||
| PRIAM | profile | ||||||||
| PDB | RCSB PDB PDBe PDBj PDBsum | ||||||||
| Ontologija gena | AmiGO / EGO | ||||||||
| |||||||||
| Fosfoglicerat kinaza | |||||
|---|---|---|---|---|---|
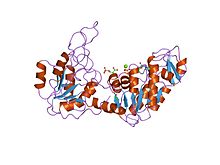 | |||||
| Struktura kvašćane fosfoglicerat kinaze.[1] | |||||
| Identifikatori | |||||
| Simbol | PGK | ||||
| Pfam | PF00162 | ||||
| InterPro | IPR001576 | ||||
| SKOP | 3pgk | ||||
| |||||
Fosfoglicerat kinaza (EC 2.7.2.3) (PGK) je enzim koji katalizuje reverzibilni transfer fosfatne grupe sa ATP-a na 3-fosfoglicerat proizvodeći ADP i 1,3-bisfosfoglicerat. Popout svih kinaza PGK je transferaza. Glukoneogeneza i Kalvinov ciklus, koji su anabolički putevi, koriste ATP i vrše reakciju u suprotnom smeru. Glikoliza, katabolički put, koristi reverznu reakciju da proizvede ATP. Postoje varijante glikolize koje ne koriste PGK.
Mehanizam i struktura
Fosfoglicerat kinaza je prisutna u svim živim organizmima i njena sekvenca je visoko konzervirana tokom evolucije. Ovaj enzim je monomer koji sadrži dva domena približno jednake veličine koji odgovaraju N- i C-kraju proteina. 3-fosfoglicerat (3-PG) se vezuje za N-terminal, dok se nukleotidni supstrati, MgATP ili MgADP, vezuju za C-terminalni domen enzima.[2] U osnovi svakog domena je šestolančana paralelna beta ravan okružena alfa heliksima. Domeni imaju sposobnost nezavisnog savijanja.[3][4]
Ljudski izozimi
|
| ||||||||||||||||||||||||||||||||||||||||||||
Deficijencija fosfoglicerat kinaze (PGK) je vezana za hemolitičku anemiju i mentalne poremećaje kod ljudi.[5]
References
- ↑ Watson HC, Walker NP, Shaw PJ, et al. (1982). „Sequence and structure of yeast phosphoglycerate kinase”. EMBO J. 1 (12): 1635–40. PMC 553262. PMID 6765200.
- ↑ Kumar S, Ma B, Tsai CJ, Wolfson H, Nussinov R (1999). „Folding funnels and conformational transitions via hinge-bending motions”. Cell Biochem. Biophys. 31 (2): 141–164. PMID 10593256.
- ↑ Yon JM, Desmadril M, Betton JM, Minard P, Ballery N, Missiakas D, Gaillard-Miran S, Perahia D, Mouawad L (1990). „Flexibility and folding of phosphoglycerate kinase”. Biochimie 72 (6-7): 417–429. PMID 2124145.
- ↑ Zerrad L, Merli A, Schröder GF, Varga A, Gráczer É, Pernot P, Round A, Vas M, Bowler MW (2011). „A spring-loaded release mechanism regulates domain movement and catalysis in phosphoglycerate kinase”. J. Biol. Chem. 286 (16): 14040-8. DOI:10.1074/jbc.M110.206813. PMC 3077604. PMID 21349853.
- ↑ Yoshida A, Tani K (1983). „Phosphoglycerate kinase abnormalities: functional, structural and genomic aspects”. Biomed. Biochim. Acta 42 (11-12): -. PMID 6689547.
Literatura
- Nicholas C. Price, Lewis Stevens (1999). Fundamentals of Enzymology: The Cell and Molecular Biology of Catalytic Proteins (Third izd.). USA: Oxford University Press. ISBN 019850229X.
- Eric J. Toone (2006). Advances in Enzymology and Related Areas of Molecular Biology, Protein Evolution (Volume 75 izd.). Wiley-Interscience. ISBN 0471205036.
- Branden C, Tooze J.. Introduction to Protein Structure. New York, NY: Garland Publishing. ISBN: 0-8153-2305-0.
- Irwin H. Segel. Enzyme Kinetics: Behavior and Analysis of Rapid Equilibrium and Steady-State Enzyme Systems (Book 44 izd.). Wiley Classics Library. ISBN 0471303097.
- Robert A. Copeland (2013). Evaluation of Enzyme Inhibitors in Drug Discovery: A Guide for Medicinal Chemists and Pharmacologists (2nd izd.). Wiley-Interscience. ISBN 111848813X.
- Gerhard Michal, Dietmar Schomburg (2012). Biochemical Pathways: An Atlas of Biochemistry and Molecular Biology (2nd izd.). Wiley. ISBN 0470146842.
Spoljašnje veze
- MeSH Phosphoglycerate+kinase
- Illustration at arizona.edu Arhivirano 2006-09-02 na Wayback Machine-u
- p
- r
- u




